Третичная структура
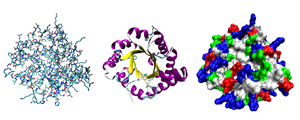
Третичная структура (или трёхмерная структура[1]) — пространственное строение (включая конформацию) всей молекулы белка или другой макромолекулы, состоящей из единственной цепи[2][3].
Третичной структурой белка называется способ укладки полипептидной цепи в пространстве. По форме третичной структуры белки делятся в основном на глобулярные и фибриллярные. Глобулярные белки чаще всего имеют эллипсовидную форму, а фибриллярные (нитевидные) белки — вытянутую (форма палочки, веретена).
Однако конфигурация третичной структуры белков еще не дает основания думать, что фибриллярные белки имеют только β-структуру, а глобулярные α-спиральные. Есть фибриллярные белки, имеющие спиральную, а не слоисто-складчатую вторичную структуру. Например, α-кератин и парамиозин (белок запирательной мышцы моллюсков), тропомиозины (белки скелетных мышц) относятся к фибриллярным белкам (имеют палочковидную форму), а вторичная структура у них — α-спираль; напротив, в глобулярных белках может быть большое количество β-структур.
Спирализация линейной полипептидной цепи уменьшает ее размеры примерно в 4 раза; а укладка в третичную структуру делает ее в десятки раз более компактной, чем исходная цепь.
Третичная структура белков
[править | править код]Связь с первичной структурой
[править | править код]Третичная структура в значительной степени определяется первичной структурой. Усилия по предсказанию третичной структуры белка, основываясь на его первичной структуре, известны как задача предсказания структуры белка. Окружающая среда, в которой белок сворачивается, существенно влияет на его конечную форму, но обычно непосредственно не принимается во внимание текущими методами предсказания. Большинство таких методов полагаются на сравнения с уже известными структурами, и таким образом учитывают влияние окружающей среды косвенно.
Стабилизирующие взаимодействия
[править | править код]В стабилизации третичной структуры белка принимают участие:
- ковалентные связи (между двумя остатками цистеина — дисульфидные мостики);
- ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
- водородные связи;
- гидрофильно-гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула «стремится» свернуться так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
Третичная структура РНК
[править | править код]Третичную структуру имеют также многие молекулы нуклеиновых кислот; в частности, универсальную третичную структуру имеют молекулы тРНК[4].
См. также
[править | править код]Литература
[править | править код]- Кузнецова И. М., Форже В., Туроверов К. К. (2005). Структурная динамика, стабильность и фолдинг белков. Цитология, т. 47, № 11, с. 943—952.
Примечания
[править | править код]- ↑ Karshikoff Andrey, «Non-covalent Interactions In Proteins» Архивная копия от 18 октября 2011 на Wayback Machine, ISBN 1-86094-707-7. Цитата: «The three-dimensional structure of proteins is often called tertiary structure», — Трёхмерную структуру белков часто называют третичной структурой.
- ↑ tertiary structure Архивная копия от 19 мая 2011 на Wayback Machine // IUPAC Gold Book.
- ↑ What are macromolecular structures? Дата обращения: 3 октября 2017. Архивировано 12 мая 2020 года.
- ↑ Строение транспортных РНК и их функция на первом (предрибосомном) этапе биосинтеза белков Архивная копия от 20 января 2012 на Wayback Machine. ФАВОРОВА О. О.